- 封面故事
- 2014年
- 533期-科學、數學,動手玩(5月號)
文章專區
2014-05-01可在客廳演示的化學遊戲—碘的氧化還原反應
533 期
Author 作者
蕭次融/臺灣師範大學化學系退休教授。
在高中的化學課程中,最容易引起學生興趣的內容,多數學生認為是化學反應。因為化學反應是物質的變化,常伴隨著令人驚訝的聲、光、色,即使教師在課堂上演示酸鹼反應,指示劑的變色或氧化還原的瞬間變色,也常能引學生的目光,但若能親自動手做實驗,更易培養興趣,而且會有很大的成就感。
本篇介紹在客廳就可演示的化學實驗,顧名思義實驗器材在家裡就可以取得,而且實驗很安全,當然學生也可以親自動手操作實驗。若操作或演示實驗時,配以有趣的旁白則更能增加實驗的可看性。因此本篇選擇碘的色變為主題,一者試劑容易取得,通常在急救箱就可找到實驗所需的碘酒與雙氧水,而且碘的顏色隨著其氧化還原的反應而變,容易引人注目,再者在化學原理上可說明一直困擾著學生的氧化還原反應以及自身氧化還原反應。另一原因在於近來在科學教育注重「POE教學」,而碘的色變可作為POE教學的良好教材。
所謂POE教學,就是在上課之前,教師要提出問題或在演示實驗之前,教師要讓學生預期(predict)可能的解答或可能產生的現象,然後教師給予解答或演示實驗,讓學生思考其解答的正確性,或觀察(observe)實驗所發生的現象,最後要求學生對於答案或所觀察到的現象給予合理的解釋(explain),而碘的色變,其實驗正可配合POE教學。以下針對碘的色變分為(一)碘的氧化還原反應、(二)碘與澱粉液的反應、(三)碘的自身氧化還原,然後綜合這三項實驗,合成一個簡而有趣的化學,亦即所謂的PAC(plain and attractive chemistry)演示實驗:(四)神奇的七個杯子。這個演示實驗宛如化學驚奇秀(wonder of chemistry shows), 以魔術手法展現chemistry magic,強調寓教於樂。因此建議讀者先演示(四)神奇的七個杯子,博取觀眾的驚訝與注意後,依(一)(二)(三)序演示並說明碘的色變原理,以達教學目標。
實驗器材
1. 碘酒(急救箱)
2. 雙氧水(急救箱)
3. 鹽酸(3M)
4. 氫氧化鈉(3M)
5. 澱粉液(0.01%或餅乾)
6. 火柴
7. 塑膠杯(透明的,8個)
8. 鐵絲(直徑約1毫米,長25公分)
說明:3、4、5項的溶液,均裝於5毫升的點滴瓶(圖一)。鹽酸可用食醋或酸性浴廁清潔劑替代,氫氧化鈉則可以小蘇打的飽和溶液或管路疏通劑替代,但用量(濃度與滴數)須調整。演示神奇的七個杯子,需要另加酚酞溶液(0.4%)或紫色高麗菜汁。
 圖一:使用的器材。
圖一:使用的器材。
(一)碘的氧化還原反應
預期
點燃的火柴,立即放入盛有碘溶液的杯中,會有何現象發生?
操作與觀察
1. 倒清水約10 毫升於透明杯中,滴入碘酒數滴至溶液呈現黃褐色。
2. 一手拿黃褐色溶液的杯子與火柴盒,並以另一個杯子的杯底當作杯蓋(圖二)。
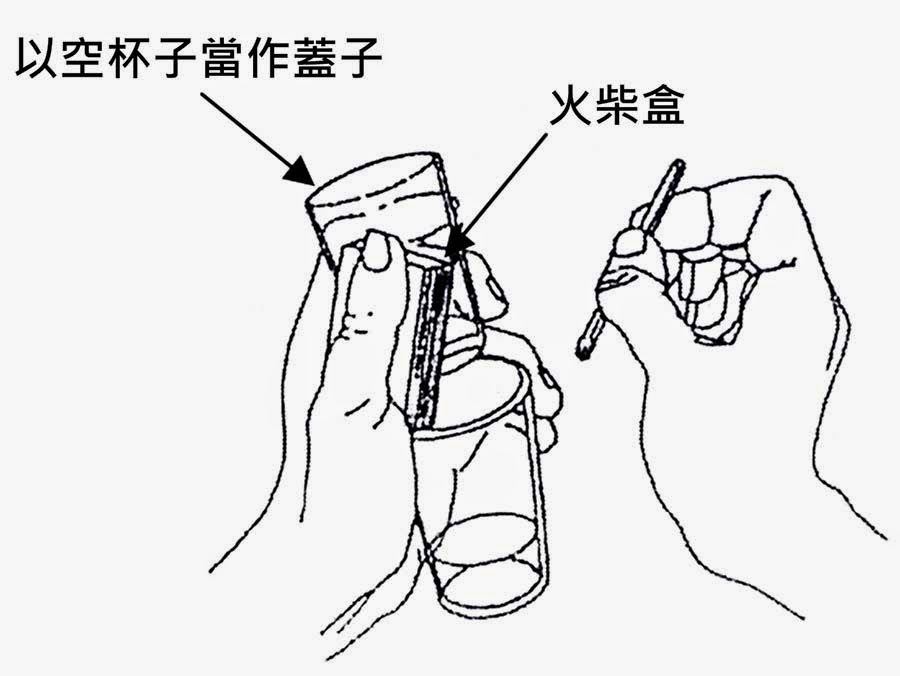
圖二:一手拿好相疊的兩個杯子與火柴盒,另一手拿火柴準備點燃火柴。
3. 點燃火柴後,立即移入杯中,但勿碰觸到溶液(圖三A與圖四)。
4. 以另一個空杯子的杯底輕蓋杯子,然後搖動杯子,即見黃褐色的碘液褪為無色(圖三B)。
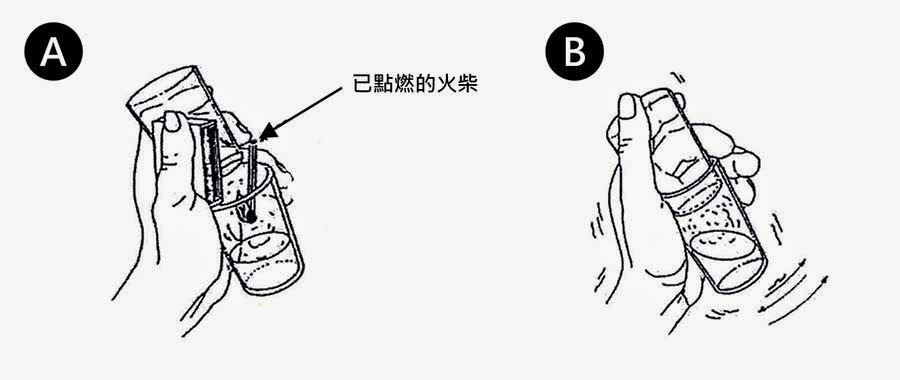
圖三:點燃火柴,以其所產生的SO2還原黃褐色的碘液為無色。
(A)點燃的火柴,立即移入杯內。
(B)輕蓋杯子後搖動杯子,碘液變為無色。
5. 如果碘液不褪為無色,重複操作步驟3、4數次至無色。
6. 在無色的溶液中,加入雙氧水數滴,過一會兒,碘的黃褐色復現。
解釋與補充說明
1. 操作3與4使黃褐色的碘液(I2 或 I3-)被點燃火柴所產生的二氧化硫(SO2,溶於水變成HSO3-;,溶解度約為11.3 克SO2/100毫升水)還原成無色的碘離子(I -)。反應式如下:
2. 操作6是在無色的溶液中加雙氧水(H2O2),因雙氧水具有氧化性,氧化了無色的碘離子為黃褐色的碘液。 ……【更多內容請閱讀科學月刊第533期】